[ 펩트론 (087010) ]
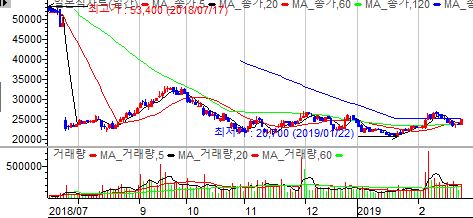
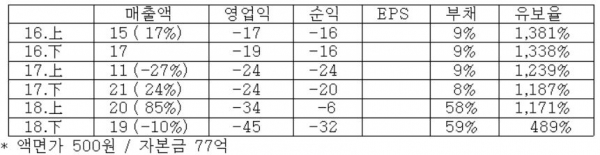
[ 1 ] 실적 분석
< 분석 결과 > * 투자의견 : 긍정적 대응
약효 지속형 제제기술인 SmartDepot라는 플랫폼을 가진 기업이다.
SmartDepot 기술은 약물의 반감기를 감소시키고, 특히 에멀젼 기술보다 훨씬 뛰어난 기능을 보유하고 있어 인체 투입과 지속성에 있어 어려움을 겪고 있는 펩타이드제제들에게 쓸모가 많고, 이들이 주로 공략하는 당뇨, 비만치료제에 유용한 기술이다.
GLP-1 제제인 Exenatide에 SmartDepot 기술을 적용해 당뇨와 비만, 파킨슨병 등의 치료물질로 개발 중이며, 여타 다른 물질에도 SmartDepot 기술을 응용할 수 있어 실질적으로 많은 파이프라인을 가진 것과 마찬가지 위치이다.
플랫폼 기술을 가진 바이오회사(펩트론, 제넥신, 신라젠 등)의 안정성 및 가능성이 돋보이기에 오히려 한두 개의 신약개발에 집중하는 제약/바이오 회사보다 프리미엄을 주는 것이 타당해 보인다.
임상 진행 및 기술이전을 위해 가장 중요했던, 오송공장에 대한 식약처의 GMP 인증을 2019년 2월에 받음으로써 2019년은 연구 성과는 물론 기술이전 등 의미있는 도약의 한 해가 될 수 있겠다.
[ 2 ] 기업 핵심 분석
( 1 ) SmartDepot 기술 : Sustained Release(SR)-DDS 기술
펩트론의 플랫폼 기술인 SmartDepot는 기존의 에멀전 방식의 한계를 극복한 펩타이드 의약품의 약효 지속형 제제기술. 펩타이드 약물(API)와 생분해성 고분자물질(Polymer)을, 약효지속성 미립구(Microsphere)로 만들어 체내에 투약 후 캐리어가 생분해되면서 약물을 지속적으로 방출시키는 기술이다.
( 2 ) SmartDepot 기술의 장점
① 주사 바늘 사이즈 축소에 유리하다.
② 약물의 구조 변형없이 물리적인 방법으로만 약물 방출속도를 조절하기에 범용성이 높다.
③ 다른 지속형 제제 대비 약물의 혈중농도 조절이 용이해 월 1회 이상의 제형 개발이 가능하다. 최대 6개월까지 가능하다.
④ 제조 재현성과 Scale up이 용이해 대량 생산시 비용 절감 측면에서 유리하다.
( 3 ) SmartDepot 기술을 적용한 파이프라인
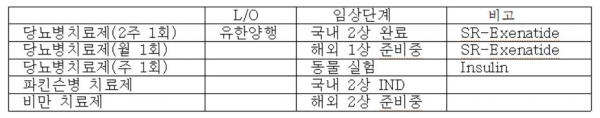
2014년 NIH와 퇴행성 뇌질환 공동연구개발(CRADA) 계약을 체결하고, NIH가 보유하고 있는 GLP-1 제제인 Exenatide의 뇌질환 용도 특허에 대한 글로벌 전용실시권을 획득했다. Smart Depot 기술을 적용하여 SR-Exenatide를 개발해 △당뇨병을 적응증으로 1~2주 1회 지속형으로 유한양행과 국내 판권계약을 맺고, 국내 임상 2상을 완료했다. 국내 임상 3상 및 해외 임상 2상 준비 중이다 △당뇨병을 적응증으로 1개월 지속형 물질을 개발하고 해외 임상 1상 준비 중이다 △파킨슨병을 적응증으로 국내 임상 2상 IND 승인을 받았다. 2019년 1분기에 110명의 110명의 파킨슨병 환자를 대상으로 주 1회 제형으로 임상 2상을 진행해 2020년 완료 예정이다 △비만치료제로 처방되고 있는 Saxenda(1일 1회 제형)와는 달리 주 1회 제형이며, 다국적사와의 제휴를 통해 2019년 상반기에 글로벌 임상 2상 예정이다.
( 4 ) 오송 SR(Sustained-Release) 1공장
① 오송 바이오파크 준공 (2018년 4월)
오송바이오파크는 시설비 200억을 투자한 cGMP 수준의 스마트 공장(건축 연면적 4700㎡ 규모)으로 연간 100만 바이알의 주사제를 생산할 수 있다.
플랫폼기술 'SmartDepot'를 적용해 다양한 펩타이드 의약품 지속기간을 1주에서 1개월까지 유지시킬 수 있는 최신 SR 약효지속성 의약품 전용 생산시설로, 세계적 수준의 무균 주사제 제조공정이 확립됐다.
② 식약처로부터 GMP 허가 획득 (2019년 2/14일)
2018년 2/14일 식약처로부터 GMP 허가를 획득했다. 이로써 임상중인 약물의 임상시료를 생산하고, SmartDepot 기반 의약품을 상업용으로 대량 생산할 수 있게 됐다.
또한 오송 GMP 공장 본격 가동으로 다양한 펩타이드 의약품에 펩트론의 SR 롱액팅 플랫폼 기술을 접목하는 기술 제휴와 신약 임상이 크게 탄력을 받을 것이다.
( 5 ) PT320 : 파킨슨병 치료제 후보물질
① 국내 임상 2상 승인 (2019년 2/18일)
오송공장 완공에 따라 식약처로부터 오송 공장에서 생산한 임상용 제품으로 임상 2상을 진행하는 시험 계획 변경승인을 받았다. PT320의 임상 2상 시험은 2020년 완료를 목표로 서울대병원과 아산병원, 삼성 서울병원에서 초기 파킨슨 질환을 가진 환자를 대상으로 진행된다.
임상시험 설계에는 펩트론 과학자문위원회(SAB) 위원으로 활동 중인 메이오 클리닉 의대 정신과와 약리학 정교수로 재직 중인 최두섭 박사가 참여했다.
② 최두섭 박사
최두섭 박사가 PT320 임상설계에 참여함에 따라 임상 수준이 세계 기준으로 향상돼 신약개발 성공 가능성을 높이는 계기가 됐다. 최 박사는 국내 임상 담당의와의 긴밀한 연계 뿐아니라 미국 국립보건연구원(NIH) 등 해외 유수의 전문가들로 구성된 공동연구망을 활용한 임상결과 분석과 논문 작성 및 학회 발표 등에도 핵심적인 역할을 할 것으로 기대된다.
( 6 ) 낮은 대주주 지분율과 100% 무상증자
최대주주이자 대표이사인 최호일씨의 지분율이 9.8%에 불과하며, 특수관계인을 모두 합친 지분율도 11.2%에 불과(2018년 9월말 현재)하다.
2018년 7/26일을 기준일로 100% 무상증자를 단행, 발행주식수가 1532만주(자본금 76.6억)로 증가했다.
( 7 ) 실적 추이